研究概要
私たちは、これまで培ってきた粘膜免疫学研究の技術を駆使して
- 粘膜間葉系リテラシー研究(SCAI project)
- アレルギー発症に関わる免疫細胞の機能切り替えスイッチの探索
- 悪玉腸内細菌に対する臓器ネットワーク
という研究テーマを進めています。社会実装を目指した共同研究や大学院生 (千葉大学大学院医学研究院入学案内)、研究員を募集しています。研究生も受け入れています。
① 粘膜間葉系リテラシー・SCAI project ~革新的な治療法の開発を目指して~
キーワード:線維化、組織修復、粘膜免疫
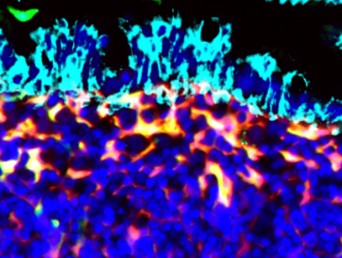
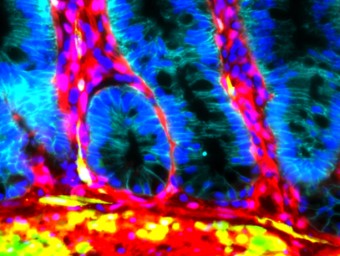
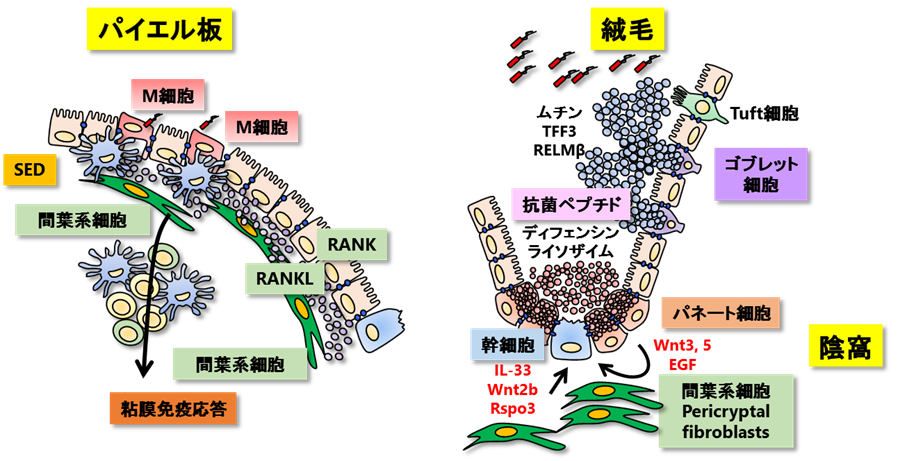
生体の最前線に位置する腸管などの粘膜組織では、粘液の産生や物理的障壁として機能する上皮細胞が重要な生体のバリア機能を担っています。その粘膜上皮細胞の支持層には、細胞外基質を産生し、組織構造の形成に必須な線維芽細胞や筋線維芽細胞といった「間葉系細胞・Structural cells」(図1参照)が分布しています。最近、このようなStructural cellが単なる支持細胞としてだけではなく、上皮細胞の分化の調整など多彩な機能をもつことが徐々に明らかになってきました(粘膜バリア後方支援)(図2参照)。
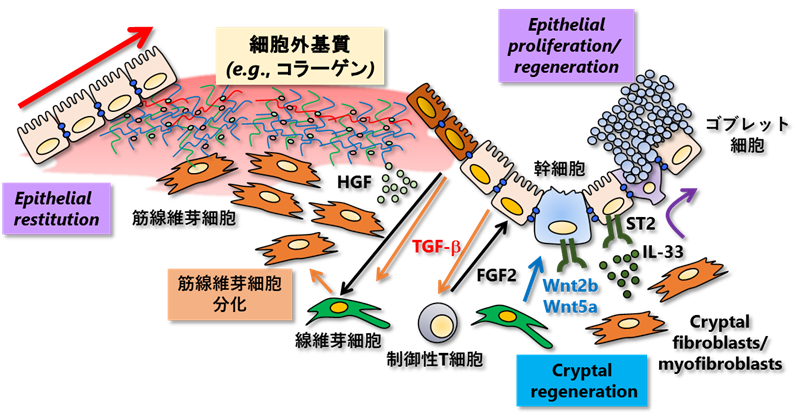
Structural cellは組織修復や臓器の機能不全の原因となる「線維化」にも深く関わっています(図3参照)。
私たちの研究室では、組織の恒常性維持や線維化などの病態形成におけるStructural cellの重要な機能を明らかにし、「免疫末梢教育」・「粘膜バリア後方支援」・「線維化」をキーワードに創薬・臨床につながる基礎研究を進めています。多彩な役割を担う間葉系細胞/Structural cellの複雑系を読み解き活用することを「粘膜間葉系リテラシー」と呼んでいます。
私たちの研究室では、2021年に炎症性腸疾患や合併症に関わる悪玉腸内細菌の組織内への侵入を抑えるための複数の臓器の連携した働き「臓器連関」を見出しました。研究テーマの一つとして「臓器ネットワークによる悪玉腸内細菌の制御機構」を明らかにし応用することで様々な組織で起こる病態の予防・治療法の確立を目指した研究も進めています。
② アレルギーに関わる免疫細胞の機能切り替えスイッチの探索~アレルギー根治を目指して~
キーワード:アレルギー、マスト細胞、免疫抑制
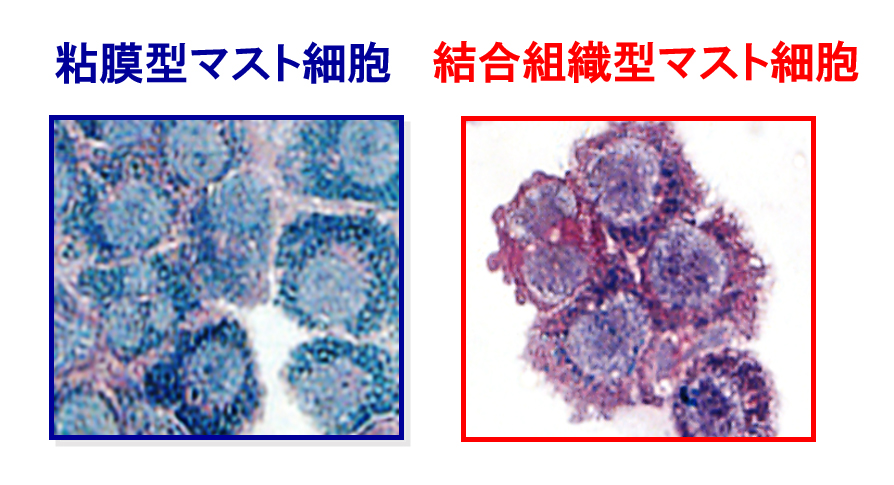
マスト細胞(肥満細胞とも呼ばれます)は、アレルギーを起こすヒスタミンなどを持つ細胞として知られてますが、未成熟な細胞として骨髄から血中を介して全身の組織内に分布した後に最終的に顆粒形成し成熟します。マスト細胞の維持にはマスト細胞上のc-kitと呼ばれる受容体とそのリガンドであるサイトカインのstem cell factorが必須であり、このどちらの分子を欠くマウスではマスト細胞ができません。このstem cell factorはStructural cellの一つである「線維芽細胞」が主たる分泌源といわれています。
マスト細胞は活性化するとコンドロイチン硫酸やプロテアーゼを放出して、寄生虫などに対する感染防御に働くといわれています。このような分泌物を細胞顆粒内に豊富に含んでいるマスト細胞は「粘膜型マスト細胞」といわれ、呼吸器、消化管でのアレルギーに関わることも知られています。私たちは、この「粘膜型マスト細胞」の誘導に間葉系細胞/Structural cellの一つの線維芽細胞が関わること(末梢教育機構)を明らかにしています(図4、5参照)。そしてこのマスト細胞の機能調節機構が破綻すると炎症が起こることもわかりました (東大プレスリリース,U Tokyo Research)。
アレルギー反応については、今から50年ほど前に発見されたIgE抗体がアレルゲンと複合体を作ってマスト細胞を活性化させることで起こることがわかっています。アレルギー疾患に対しては抗ヒスタミン、抗ロイコトリエンまたはIgEといったマスト細胞からの分泌物や活性化を抑える対症療法が主です。特に、粘膜面ではこの「粘膜型マスト細胞」の機能を抑えることが大切になってきます。そこで私たちは、単に「粘膜型マスト細胞」の活性化を抑えるのではなく、逆にアレルギーを抑えるような性質へと変える「機能スイッチ分子」を探し、抗アレルギー型のマスト細胞へと変換する試みを進めています。
2020年には、リバーストランスレーショナルリサーチの一環として、食物アレルギーの臨床研究段階の治療法の「経口免役療法」の実験モデルをつくり、マスト細胞の「抗アレルギー作用」を見出しました。
アレルギーの発症に関わり悪玉細胞であるマスト細胞を「善玉細胞」に置き換えることができれば、新たなアレルギー治療につながると期待しています。
New era for mucosal mast cells.
Two sides of the coin: Mast cells as a key regulator of allergy and acute/chronic
inflammation.